Seguridad, reactogenicidad e inmunogenicidad de FINLAY-FR-1A y FINLAY-FR-1: resultados de un ensayo clínico de fase I aleatorizado y doble ciego
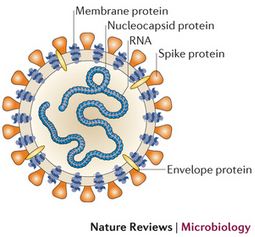
 La glicoproteína S trimérica media la unión a la enzima convertidora de angiotensina humana (hACE2) en la superficie de las células huésped. La proteína S tiene dos subunidades: S1 y S2. S1 media la unión de hACE2 a través del dominio de unión al receptor (RBD: Receptor Binding Domain), mientras que S2 media la fusión viral.
La glicoproteína S trimérica media la unión a la enzima convertidora de angiotensina humana (hACE2) en la superficie de las células huésped. La proteína S tiene dos subunidades: S1 y S2. S1 media la unión de hACE2 a través del dominio de unión al receptor (RBD: Receptor Binding Domain), mientras que S2 media la fusión viral.
Los anticuerpos neutralizantes contra el SARS-CoV-2 son estimulados principalmente por el RBD, mientras que otras proteínas del SARS-CoV-2 pueden promover un mecanismo inmunopatogénico mediado por anticuerpos conocido como ADE (Antibody Dependent Enhancement). El bloqueo de la interacción RBD-hACE2 es el objetivo principal de las vacunas contra el SARS-CoV-2.
Se han desarrollado varias vacunas, basadas en diferentes plataformas. La Organización Mundial de la Salud (OMS) ha aprobado el uso de vacunas de virus inactivados, vacunas de vectores de adenovirus y vacunas de ARNm, que han demostrado su eficacia frente a la COVID-19, especialmente las basadas en nuevas tecnologías; sin embargo, han planteado problemas de seguridad. Otro enfoque ha sido el desarrollo de vacunas de subunidades de proteínas, en particular aquellas que utilizan el RBD de la proteína espiga del SARS-CoV-2.
FINLAY-FR-1 (SOBERANA 01) y FINLAY-FR-1A (SOBERANA Plus) son candidatos vacunales basados en un dímero RDB recombinante (d-RBD). Se producen bajo condiciones de Buenas Prácticas de Manufactura en el Instituto de Vacunas Finlay y el Centro de Inmunología Molecular, en La Habana, Cuba; ambos terminaron las evaluaciones preclínicas y toxicológicas. Este estudio evaluó la seguridad y la reactogenicidad de FINLAY-FR-1A y FINLAY-FR-1-formulaciones que hoy conocemos como Soberana Plus y Soberana 01- comparó la inmunogenicidad inducida por tres dosis de estas vacunas candidatas.
Vea el artículo completo en:





 Las infecciones provocadas por los coronavirus son comunes en todo el mundo y pueden afectar a personas y animales. En los humanos pueden causar el catarro común y la gastroenteritis en lactantes. Existen varios tipos de coronavirus y aunque por lo general ocasionan enfermedades leves o moderadas, también pueden estar implicados en procesos graves...
Las infecciones provocadas por los coronavirus son comunes en todo el mundo y pueden afectar a personas y animales. En los humanos pueden causar el catarro común y la gastroenteritis en lactantes. Existen varios tipos de coronavirus y aunque por lo general ocasionan enfermedades leves o moderadas, también pueden estar implicados en procesos graves... 


Comentar