Vacunas contra el SARS-CoV-2: duración de la inmunidad
 La duración de la imunidad que generan las vacunas contra el SARS-CoV-2 es un tema en constante revisión en la literatura científica.
La duración de la imunidad que generan las vacunas contra el SARS-CoV-2 es un tema en constante revisión en la literatura científica.
Las vacunas de ARN han surgido como una herramienta poderosa en la lucha contra la pandemia de COVID-19, demostrando ventajas significativas como la capacidad de fabricación a gran escala y un costo razonable, lo que las hace accesibles a los países en desarrollo y subdesarrollados, y creando un impacto global positivo.
Los diferentes tipos de ARN, incluido el ARNm convencional, el ARNm autoamplificado y el ARN circular, ofrecen distintas ventajas y desafíos. El ARNm convencional es seguro para la administración y se fabrica fácilmente mediante transcripción in vitro (IVT); sin embargo, es posible que no siempre provoque la respuesta inmunitaria deseada, lo que requiere el uso de un sistema de administración eficaz. El ARNm autoamplificado aborda esta limitación al permitir la expresión suficiente de antígenos a través de su proceso de autoamplificación, pero el uso de elementos de alfavirus puede plantear problemas de seguridad e inducir respuestas inmunitarias no deseadas.
El ARN circular es prometedor debido a su estabilidad inherente, lo que resulta en una vida media del ARN más larga y una expresión prolongada del antígeno sin requerir un sistema de administración. Sin embargo, su complejo proceso de fabricación y la circulación limitada del ARN plantean desafíos.
Además, en algunas circunstancias, las vacunas de ARN pueden resultar difíciles de implementar, ya que en áreas con recursos limitados o de bajos ingresos, la pobreza crea barreras de costos para aquellas regiones que utilizan esta tecnología avanzada. Las vacunas de ARN pueden ser más caras de producir y distribuir si requieren liofilización o transporte en cadena de frío para estabilizarse. A pesar de estos desafíos, las vacunas de ARNm han logrado hitos importantes no solo en la pandemia de SARS-CoV-2 sino también en la lucha contra otros patógenos.
La duración de la protección y, por lo tanto, la necesidad de dosis adicionales son inciertas. Tampoco está claro en qué medida la reducción de la eficacia de la vacuna es resultado de una nueva variante o de una disminución de la inmunidad.
Los datos de inmunogenicidad indican que los títulos de anticuerpos disminuyen relativamente rápido después de recibir dos dosis de vacuna, lo que sugiere que la disminución puede ser un factor importante en las reducciones notificadas de la eficacia de la vacuna con el tiempo, aunque las disminuciones de los títulos de anticuerpos pueden ser más rápidas que las disminuciones de la protección.
Se ha descubierto que varios marcadores serológicos se correlacionan con la infección por SARS-CoV-2, pero no con la COVID-19 grave o mortal. Además de la aparición de la variante delta más transmisible, la disminución de la protección contra la infección sintomática a medida que aumenta el tiempo desde la vacunación también contribuyó probablemente al aumento de la incidencia de la COVID-19 en algunos lugares.
También se plantean importantes interrogantes sobre el momento de administrar una tercera dosis de la vacuna a los adultos que siguen protegidos contra la hospitalización y la muerte durante al menos cinco meses después de recibir dos dosis. Israel fue uno de los primeros países en inmunizar a los adultos con la vacuna BNT162b2 y comenzó a ofrecer una tercera dosis de la misma vacuna a los adultos mayores a partir de julio de 2021. Los primeros datos de sus resultados indican que la tercera dosis se asoció con grandes reducciones en la incidencia de la infección por SARS-CoV-2 en la semana posterior a la vacunación, y con mayores reducciones en la segunda semana. Sin embargo, la duración de la protección ofrecida por la tercera dosis aún es incierta.
Una tercera dosis de la vacuna mejora la inmunidad humoral y celular contra el SARS-CoV-2, con una mayor actividad neutralizante contra diferentes variantes, incluida la variante delta, que probablemente mejore la protección contra la infección. En algunos estudios de cohorte, la disminución de la eficacia de la vacuna contra los resultados de enfermedad grave fue relativamente limitada, pero es probable que continúe con el tiempo desde la recepción de dos dosis de la vacuna.
Las decisiones sobre el momento de la tercera dosis deben equilibrar la tasa de disminución de la inmunidad con la prevalencia de la enfermedad, incluido el riesgo de nuevas variantes, y la priorización de las personas con mayor riesgo de enfermedad grave. La evidencia existente sugiere que la eficacia de la vacuna aumenta con intervalos más largos entre dosis y, si esto también se aplica a las terceras dosis, también será necesario considerar el intervalo de administración.
Algunos estudios mostraron que la eficacia de la vacuna para las vacunas de adenovirus (en comparación con las de ARNm) contra las infecciones fue menor en general. Por el contrario, ambas clases de vacunas fueron similares en términos de hospitalizaciones y mortalidad. Sin embargo, no hay suficientes estudios de este tipo para sacar conclusiones y por lo tanto, es difícil afirmar que existe alguna diferencia entre las dos clases.
Dada la efectividad inicial adecuada de la vacuna contra la variante ómicron y la disminución de la efectividad de la vacuna con el tiempo, otras medidas de control de la COVID-19 (por ejemplo, el uso de mascarillas, el distanciamiento físico y la cuarentena) podrían seguir siendo necesarias para reducir la propagación del virus y reducir las hospitalizaciones y muertes relacionadas con esta infección.
Una preocupación con respecto a esta rápida expansión de la literatura, y la situación del SARS-CoV-2 en sí, es el cambio de enfoque de la investigación con cualquier nueva variante de interés que muestre diferentes características virológicas y clínicas. Las vacunas desarrolladas para una variante podrían tener una eficacia limitada para otra variante, especialmente debido a las mutaciones en la proteína de pico específica, que difiere significativamente entre variantes.
Aún faltan datos sobre varias vacunas administradas a tamaños de población significativos -por ejemplo, Covaxin (BBV152) en la India o Convidecia (Ad5-nCoV) principalmente en China- y, posiblemente, esquemas de aplicación heterólogos. Asimismo, si bien los estudios incluyen a los niños y adolescentes entre los subgrupos de vulnerabilidad por separado (una clasificación basada principalmente en términos médicos generales más que en la carga de enfermedad de COVID-19 en sí), no sucede así para otros subgrupos de edad porque los subgrupos de ancianos a menudo se informan en publicaciones sobre la población general, y se pueden pasar por alto si no se presentaran en el resumen, provocando una visión incompleta de este grupo.
De hecho, resulta muy importante la representación de estudios que incluyan a ancianos que se han visto amenazados por altas tasas de mortalidad por COVID-19 y, al menos teóricamente, pueden estar en riesgo de una respuesta inmune más débil a la vacunación debido a la edad.
La publicación de revisiones de gran alcance podría ayudar a estimular la investigación para cerrar estas brechas de conocimiento, lo que es extremadamente importante para evitar cursos graves de la enfermedad.
Recomendamos:
- Zhou, W., Jiang, L., Liao, S., Wu, F., Yang, G., Hou, L., Liu, L., Pan, X., Jia, W., & Zhang, Y. (2023). Vaccines’ New Era-RNA Vaccine. Viruses, 15(8), 1760.
- Andrews, N., Tessier, E., Stowe, J., Gower, C., Kirsebom, F., Simmons, R., Gallagher, E., Thelwall, S., Groves, N., Dabrera, G., Myers, R., Campbell, C. N. J., Amirthalingam, G., Edmunds, M., Zambon, M., Brown, K., Hopkins, S., Chand, M., Ladhani, S. N., Ramsay, M., … Lopez Bernal, J. (2022). Duration of Protection against Mild and Severe Disease by Covid-19 Vaccines. The New England journal of medicine, 386(4).
- Wu, N., Joyal-Desmarais, K., Ribeiro, P. A. B., Vieira, A. M., Stojanovic, J., Sanuade, C., Yip, D., & Bacon, S. L. (2023). Long-term effectiveness of COVID-19 vaccines against infections, hospitalisations, and mortality in adults: findings from a rapid living systematic evidence synthesis and meta-analysis up to December, 2022. The Lancet. Respiratory medicine, 11(5), 439–452.
- Kreuzberger, N., Hirsch, C., Andreas, M., Böhm, L., Bröckelmann, P. J., Di Cristanziano, V., Golinski, M., Hausinger, R. I., Mellinghoff, S., Lange, B., Lischetzki, T., Kappler, V., Mikolajewska, A., Monsef, I., Park, Y. S., Piechotta, V., Schmaderer, C., Stegemann, M., Vanshylla, K., Weber, F., … Skoetz, N. (2022). Immunity after COVID-19 vaccination in people with higher risk of compromised immune status: a scoping review. The Cochrane database of systematic reviews, 8(8), CD015021.





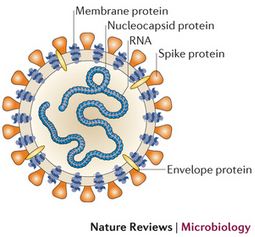
 Las infecciones provocadas por los coronavirus son comunes en todo el mundo y pueden afectar a personas y animales. En los humanos pueden causar el catarro común y la gastroenteritis en lactantes. Existen varios tipos de coronavirus y aunque por lo general ocasionan enfermedades leves o moderadas, también pueden estar implicados en procesos graves...
Las infecciones provocadas por los coronavirus son comunes en todo el mundo y pueden afectar a personas y animales. En los humanos pueden causar el catarro común y la gastroenteritis en lactantes. Existen varios tipos de coronavirus y aunque por lo general ocasionan enfermedades leves o moderadas, también pueden estar implicados en procesos graves... 


Comentar