 La Organización Mundial de la Salud y Unitaid, con el apoyo de Medicines Law and Policy, han publicado un documento informativo para facilitar el acceso de los países a tratamientos asequibles contra la COVID-19. Ver más…
La Organización Mundial de la Salud y Unitaid, con el apoyo de Medicines Law and Policy, han publicado un documento informativo para facilitar el acceso de los países a tratamientos asequibles contra la COVID-19. Ver más…
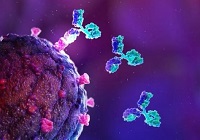 Las pautas de tratamiento y las autorizaciones de uso de emergencia (EUA) de anticuerpos monoclonales (mAb) de la Administración de Alimentos y Medicamentos de EE. UU. (FDA) para el tratamiento de pacientes ambulatorios de alto riesgo con COVID-19 de leve a moderado cambiaron con frecuencia a medida que surgieron diferentes variantes de SARS-CoV-2. Ver más…
Las pautas de tratamiento y las autorizaciones de uso de emergencia (EUA) de anticuerpos monoclonales (mAb) de la Administración de Alimentos y Medicamentos de EE. UU. (FDA) para el tratamiento de pacientes ambulatorios de alto riesgo con COVID-19 de leve a moderado cambiaron con frecuencia a medida que surgieron diferentes variantes de SARS-CoV-2. Ver más…
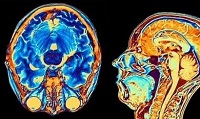 La trombosis cerebral de seno venoso, es una enfermedad poco común que afecta el drenaje venoso del cerebro entre los factores de riesgo podemos encontrar la infección por SARS-CoV-2 causante del síndrome respiratorio agudo grave, que crea un estado de hipercoagulopatía sistémica.
La trombosis cerebral de seno venoso, es una enfermedad poco común que afecta el drenaje venoso del cerebro entre los factores de riesgo podemos encontrar la infección por SARS-CoV-2 causante del síndrome respiratorio agudo grave, que crea un estado de hipercoagulopatía sistémica. 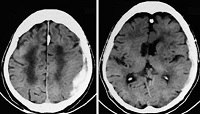 La enfermedad covid-19 exhibe una tasa de letalidad en pacientes de 80 años de edad o más del 15 %. En Italia alcanzó el 52,5 % y puede aumentar en presencia de comorbilidades. El hematoma subdural agudo presenta una mortalidad que oscila entre el 40 y el 90 %
La enfermedad covid-19 exhibe una tasa de letalidad en pacientes de 80 años de edad o más del 15 %. En Italia alcanzó el 52,5 % y puede aumentar en presencia de comorbilidades. El hematoma subdural agudo presenta una mortalidad que oscila entre el 40 y el 90 %  A pesar de la evidencia circunstancial de la propagación del SARS-CoV-2 por aerosoles y fómites, los datos empíricos que vinculan cualquiera de las vías con la transmisión son escasos.
A pesar de la evidencia circunstancial de la propagación del SARS-CoV-2 por aerosoles y fómites, los datos empíricos que vinculan cualquiera de las vías con la transmisión son escasos. 





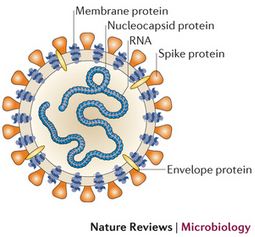
 Las infecciones provocadas por los coronavirus son comunes en todo el mundo y pueden afectar a personas y animales. En los humanos pueden causar el catarro común y la gastroenteritis en lactantes. Existen varios tipos de coronavirus y aunque por lo general ocasionan enfermedades leves o moderadas, también pueden estar implicados en procesos graves...
Las infecciones provocadas por los coronavirus son comunes en todo el mundo y pueden afectar a personas y animales. En los humanos pueden causar el catarro común y la gastroenteritis en lactantes. Existen varios tipos de coronavirus y aunque por lo general ocasionan enfermedades leves o moderadas, también pueden estar implicados en procesos graves... 


Nuestros lectores comentan